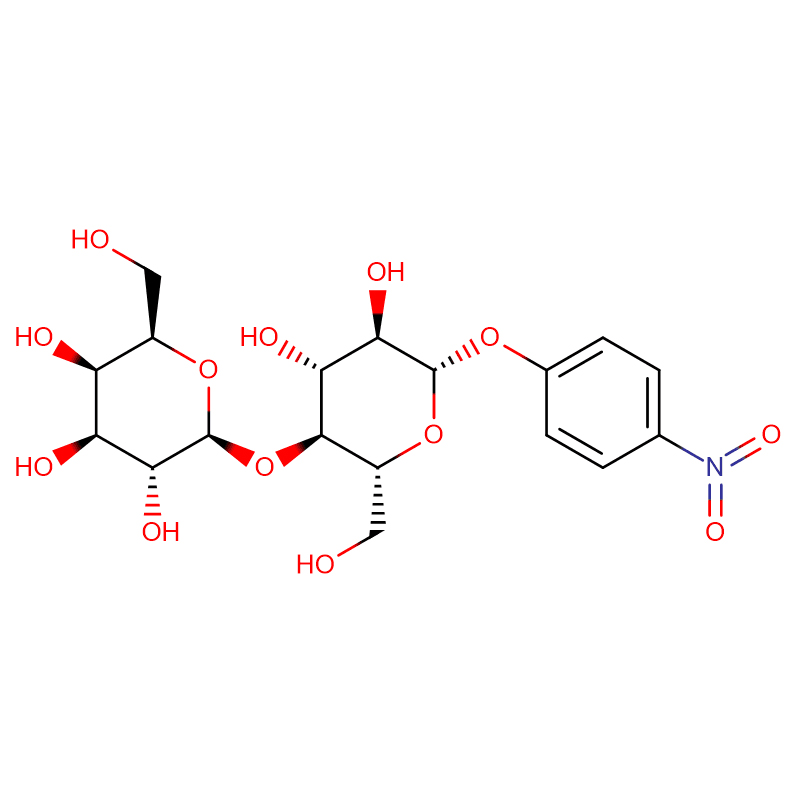
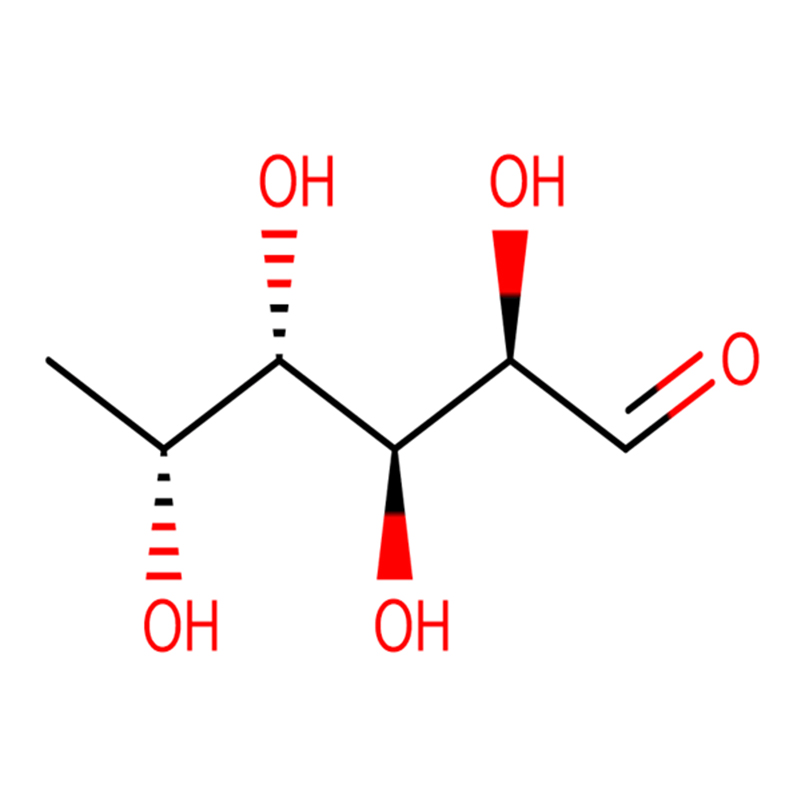
A glikozidáz inhibitor galaktovalidamin két izomer biciklo[4.1.0]heptán analógja, (1R*,2S,3S,4S,5S,6S*)-5-amino-1-(hidroxi-metil)biciklo[4.1.0]heptán A -2,3,4-triolt 13 lépésben szintetizálták 2,3,4,6-tetra-O-benzil-D-galaktózból.A két konformációslag korlátozott amin és a megfelelő acetamidok gátló aktivitását kávébabból és E. coli-ból származó, kereskedelmi forgalomban lévő alfa-galaktozidáz enzimekkel szemben mértük.A glikozil-hidroláz családba tartozó GH27 enzim (kávébab) aktivitását kompetitív módon gátolta az 1R,6S-amin (7), amely kötési kölcsönhatás 0,541 mikroM K(i) értékkel jellemezhető.A GH36 E. coli alfa-galaktozidáz sokkal gyengébb kötési kölcsönhatást mutatott az 1R,6S-aminnal (IC(50)=80 mikroM).A diasztereomer 1S,6R-amin (9) gyengén kötődött mindkét galaktozidázhoz (kávébab, IC(50)=286 mikroM) és (E. coli, IC(50)=2,46 mM).