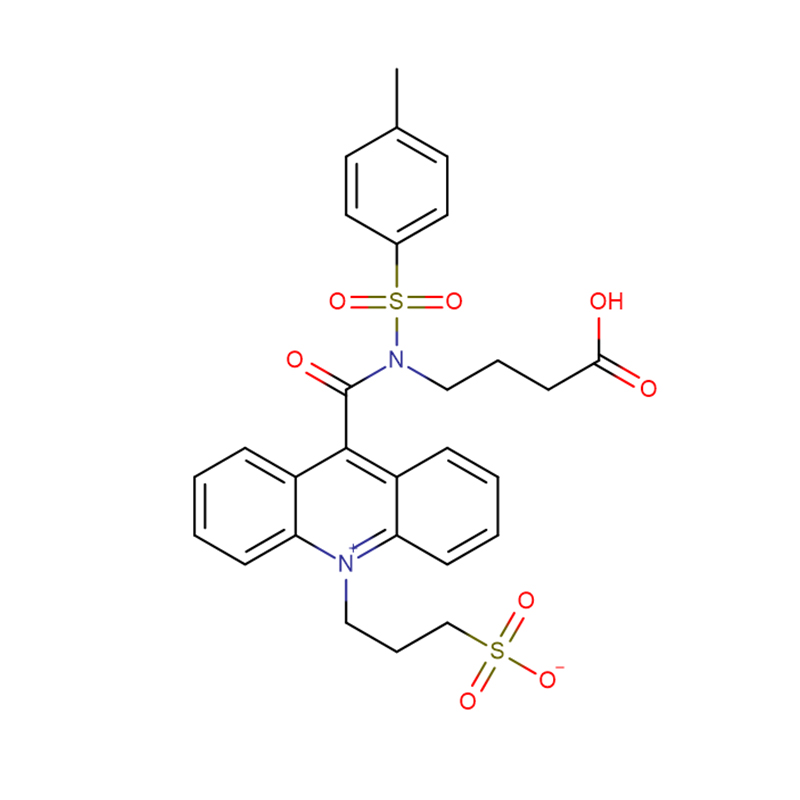
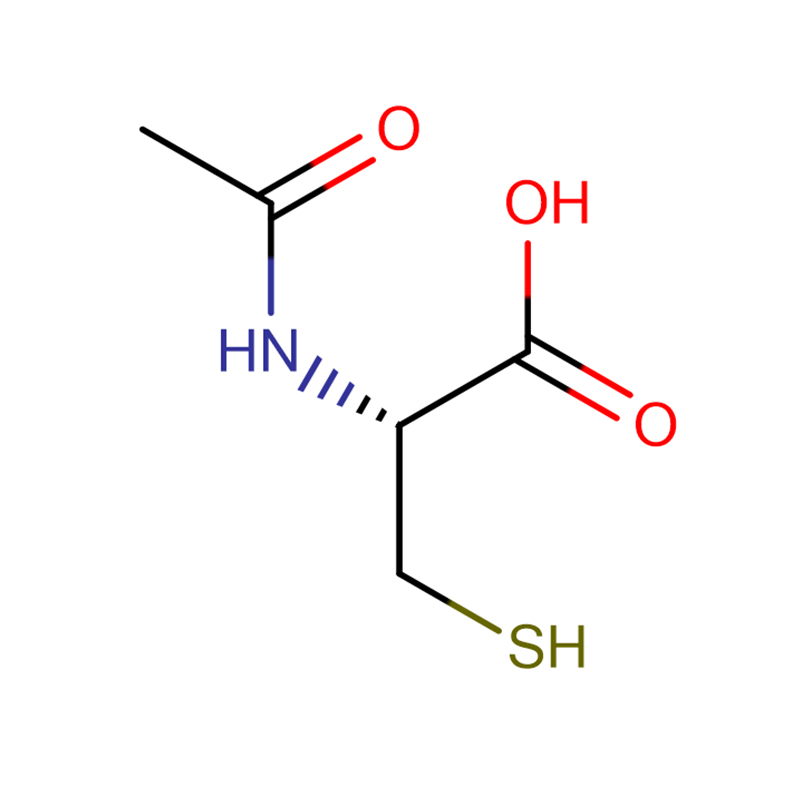
4-Amino-3-hidrazino-1,2,4-triazol-5-tiol Cas:28836-03-5 99% Sárgától zöldig terjedő szilárd anyag
| Katalógus szám | XD90146 |
| termék név | 4-amino-3-hidrazino-1,2,4-triazol-5-tiol |
| CAS | 28836-03-5 |
| Molekuláris képlet | C16H13NO3S·NH3 |
| Molekuláris tömeg | 316,37 |
| Tárolási részletek | Környező |
| Harmonizált Vámkódex | 2923900090 |
Termékleírás
| Kinézet | Sárgától zöldig terjedő szilárd anyag |
| Assay | ≥ 99% |
| Olvadáspont | 237°C (bomlik) (megl.) |
| Oldhatóság | NaOH: oldható 1 N |
| Vízben oldódó | Vízben, 1 N NaOH-ban és metanolban oldódik. |
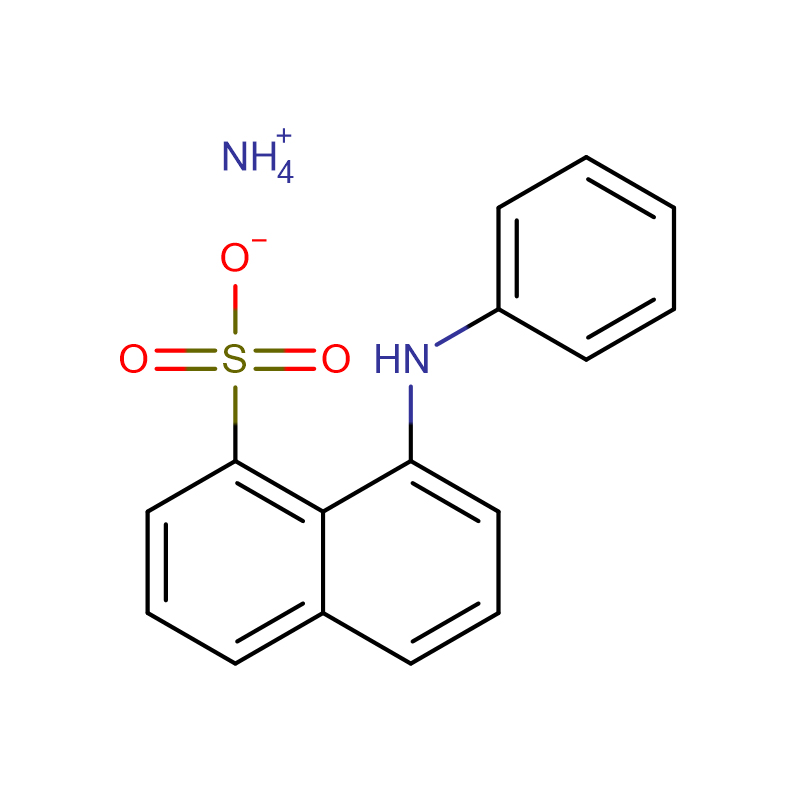
1. Gátlási kinetikával és számítógépes szimulációval vizsgáltuk az izorhamnetin gomba tirozináz gátló hatását.Az izorhamnetin kevert módon reverzibilisen gátolta a tirozinázt Ki=0,235±0,013 mM értéknél.Az intrinsic és az 1-anilinonaftalin-8-szulfonát(ANS)-kötő fluoreszcencia mérései azt mutatták, hogy az izorhamnetin nem indukált jelentős változást a tirozináz harmadlagos szerkezetében.Az inaktivációs folyamatba való betekintés érdekében a kinetikát időintervallum mérésekkel és folyamatos szubsztrát reakciókkal számítottuk ki.Az eredmények azt mutatták, hogy az izorhamnetin által kiváltott inaktiváció elsőrendű reakció volt kétfázisú folyamatokkal.A további betekintés érdekében szimuláltuk a tirozináz és az izorhamnetin közötti dokkolást.A szimuláció sikeres volt (a kötési energiák a Dock6.3 esetében: -32,58 kcal/mol, az AutoDock 4.2 esetében: -5,66 kcal/mol és a Fred2.2 esetében: -48,86 kcal/mol), ami arra utal, hogy az izorhamnetin több maradékkal is kölcsönhatásba lép, mint pl. mint a HIS244 és a MET280.Ez a tirozináz kölcsönhatás előrejelzésének stratégiája a flavanonvegyületen alapuló kinetikával kombinálva hasznosnak bizonyulhat a potenciális természetes tirozináz inhibitorok szűrésében.
2. A tyúktojásfehérjéből származó monomer glikoprotein, a konalbumin (CA) savkibontakozási útját távoli és közeli UV CD spektroszkópiával, belső fluoreszcencia emisszióval, külső fluoreszcencia szondával, 1-anilino-8-naftalin-szulfonáttal (ANS) vizsgálták. és dinamikus fényszórás (DLS).A CA másodlagos és harmadlagos szerkezetében pH-függő változásokat figyeltünk meg.Natív jellegű α-helikális másodlagos szerkezetű 4,0 pH-n, de veszteséges szerkezete 3,0 pH-n.A CA kizárólag olvadás előtti gömbölyű állapotként és olvadt golyós állapotként létezett oldatban pH 4,0 és pH 3,0 esetén.A pH hatása a CA konformációjára és termostabilitására a semleges pH melletti hőállóság felé mutat.A DLS eredmények azt mutatják, hogy az MG állapot kompakt formában létezett 4,7 nm-es hidrodinamikai sugarú vizes oldatokban.A triptofán fluoreszcenciájának akrilamiddal történő kioltása tovább erősítette egy köztes állapot felhalmozódását, részben fel nem hajtva, a natív és a fel nem hajtott állapotok között.




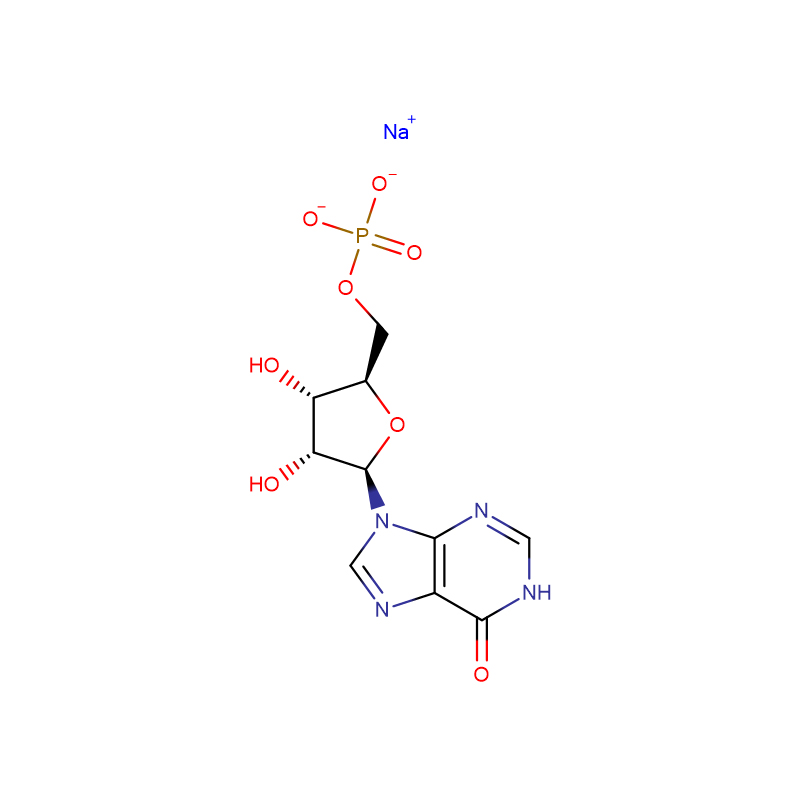
![N-[[bisz[4-(dimetilamino)fenil]amino]karbonil]glicin-nátriumsó Fehértől szürkészöldig terjedő kristályos por](http://cdn.globalso.com/xdbiochems/115871-19-7.jpg)